
2. पदार्थ का वर्गीकरण
रासायनिक संरचना के आधार पर पदार्थ को तीन वर्गों में बाँटा गया है— तत्त्व, यौगिक और मिश्रण
तत्त्व— तत्त्व पदार्थ का शुद्ध और सरलतम रूप है जिसे किसी भी भौतिक या रासायनिक विधि से दो या दो से अधिक सरल द्रव्यों में विभाजित नहीं किया जा सकता है। जैसे- हाइड्रोजन, ऑक्सीजन, लोहा, ताँबा, चाँदी आदि।
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
तत्त्व की विशेषताएं
यह एक ही प्रकार के परमाणुओं से बना होता है।
अन्य तत्त्वों के गुणों से भिन्न किसी तत्त्व के कुछ विशिष्ट गुण होते हैं। हाइड्रोजन एक तत्त्व है क्योंकि
(क) यह किसी भी भौतिक व रासायनिक विधि द्वारा दो या अधिक सरल द्रव्यों में विभाजित नहीं किया जा सकता है। (ख) यह सिर्फ हाइड्रोजन परमाणुओं का ही बना होता है जिनकी परमाणु संख्या 1 होती है।
अब तक 114 तत्त्वों का आविष्कार हो चुका है जिनमें से 92 तत्त्व प्रकृति में पाए जाते हैं जबकि अन्य संश्लेषित तत्त्व है।
तत्त्वों का वर्गीकरण
तत्त्व मुख्यतः दो प्रकार के होते हैं— धातु और अधातु
तत्त्वों की एक तीसरी श्रेणी भी होती है जिन्हें उपधातु कहते हैं। उपधातुओं के गुण धातुओं और अधातुओं के गुण के मध्यवर्ती होते हैं।
धातुओं के गुण— (क) धातुओं में एक विशेष प्रकार की चमक होती है जिसे धातुई चमक कहते हैं।
(ख) यह ऊष्मा और विद्युत के सुचालक होती है।
(ग) ठोस अवस्था में ये आघातवर्धनीय और तन्य होती हैं। अधिकांश धातुएँ कमरे के ताप पर ठोस होती हैं। पारा एक अपवाद है, जो कमरे के ताप पर द्रव के रूप में पाया जाता है।
सोडियम, तांबा, सोना, चांदी, लोहा आदि धातुओं के उदाहरण हैं।
अधातुओं के गुण— (क) अधातु में कोई विशेष प्रकार की चमक नहीं होती है। आयोडीन एक अपवाद है, जो चमकीला होता है।
(ख) ये ऊष्मा और विद्युत की कुचालक होती है।
(ग) ये प्रायः गैस या ठोस के रूप में पाई जाती है। ब्रोमीन एक ऐसी अधातु है जो द्रव रूप में पाई जाती है।
यौगिक— यौगिक वह शुद्ध पदार्थ है जो दो या अधिक तत्त्वों के भार के विचार से एक निश्चित अनुपात में रासायनिक संयोग के फलस्वरुप बनता है।
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
यौगिक को किसी रासायनिक क्रिया द्वारा विघटित करके दो या अधिक सरल तत्त्व प्राप्त किए जा सकते हैं। कैल्शियम ऑक्साइड (CaO) एक यौगिक है जो कैल्शियम (Ca) और ऑक्सीजन (O) के सहयोग से बना होता है। इसी प्रकार, हाइड्रोजन और ऑक्सीजन के सहयोग से जल एक यौगिक है जिसका रासायनिक सूत्र H2O होता है। अमोनिया (NH3), कार्बन डाइऑक्साइड (CO2) चूना पत्थर (CaCO3) आदि यौगिक के उदाहरण हैं!
यौगिक के प्रमुख गुण—
यौगिक के प्रमुख गुण निम्नलिखित हैं—
(क) यौगिक के अवयवी तत्त्वों को किसी भी यांत्रिक या भौतिक विधि द्वारा अलग अलग नहीं किया जा सकता है।
(ख) किसी यौगिक के गुण उसके अवयवी तत्त्वों के गुणों से बिल्कुल भिन्न होते हैं।
(ग) किसी यौगिक के बनने में ऊष्मा या प्रकाश के रूप में ऊर्जा का प्राय: उत्सर्जन या अवशोषण होता है।
(घ) यौगिक में उसके अवयवी तत्त्व भार के विचार से एक निश्चित अनुपात में रहते हैं।
(ङ) यौगिक के द्रवनांक और क्वथनांक निश्चित होते हैं।
मिश्रण— मिश्रण वह पदार्थ है जो दो या अधिक तत्त्व या यौगिक को किसी भी अनुपात में परस्पर मिला देने से बनता है और इसके अवयवों को सरल यांत्रिक विधियों द्वारा अलग किया जा सकता है।
जैसे- (क) वायु- यह नाइट्रोजन, ऑक्सीजन, कार्बन डाइऑक्साइड, जलवाष्प आदि का मिश्रण है।
बारूद- यह शोरा (पोटैशियम नाइट्रेट) गंधक और कोयले का मिश्रण होता है।
मिश्रण शुद्ध पदार्थ नहीं होता है। मिश्रण में उपस्थित शुद्ध पदार्थ को उनके अवयव कहते हैं।
मिश्रण के गुण—
(क) मिश्रण समांग या विषमांग हो सकता है।
उदाहरण : जल में चीनी का विलयन एक समांग मिश्रण है। इस विलयन के किसी भी भाग में चीनी और जल का अनुपात एक समान रहता है। इसमें चीनी और जल के कण अलग-अलग नहीं दिखाई देते हैं।
दो मिश्रणीय द्रवों का मिश्रण भी समांग होता है। जैसे- अल्कोहल में जल का मिश्रण।
बालू और साधारण नमक का मिश्रण विषमांगी होता है।
तेल और जल का मिश्रण भी विषमांग होता है।
(ख) मिश्रण के अवयवों को छानना, वाष्पन, उर्ध्वपातन और चुंबकीय पृथक्करण आदि भौतिक विधियों द्वारा अलग-अलग किया जा सकता है। मिश्रण के बनने में प्राय: उर्जा का न तो उत्सर्जन होता है और ना ही अवशोषण।
मिश्रण का संघटन निश्चित नहीं होता है। अर्थात मिश्रण के विभिन्न भागों में उसके अवयवों का अनुपात भिन्न होता है।
मिश्रण के द्रवनांक, क्वथनांक आदि निश्चित नहीं होते हैं।
मिश्रण के बनने में कोई रसायनिक अभिक्रिया नहीं होती है।
भौतिक और रासायनिक परिवर्तन
प्रकृति में होने वाले परिवर्तनों को दो भागों में बांटा जा सकता है— भौतिक और रासायनिक भौतिक परिवर्तन
भौतिक परिवर्तन— ऐसा परिवर्तन जिसमें पदार्थ के कुछ गुणों में थोड़ा अस्थाई परिवर्तन हो तथा इस परिवर्तन के फलस्वरुप कोई नया पदार्थ नहीं बनता हो, उसे भौतिक परिवर्तन कहते हैं।
जैसे— जल का वाष्प बनना, नमक का जल में विलयन, विद्युत बल्ब से प्रकाश का उत्सर्जन आदि।
रसायनिक परिवर्तन— रसायनिक परिवर्तन वह है जिसमें कोई पदार्थ नया पदार्थ में बदल जाता है जिसके गुण मूल पदार्थ से पूरी तरह अलग होते हैं। रसायनिक परिवर्तन को फिर से वापस मूल अवस्था में नहीं लाया जा सकता है।
जैसे- लोहे में जंग लगना, कोयले का जलना, लोहे और गंधक के मिश्रण को गर्म करना, शरीर में भोजन का पचना आदि।
विलयन— दो या अधिक पदार्थों का समांग मिश्रण विलयन कहलाता है। समांग का अर्थ है विलयन के सभी भागों में एकरूपता।
विलायक— जिस द्रव में किसी पदार्थ को घुलाया जाता है उस द्रव को विलायक कहते हैं। विलयन में विलायक परिक्षेपण माध्यम कहलाता है
विलेय— जो पदार्थ जल में घुलकर विलयन बनाता है वह विलेय कहलाता है। विलयन में विलेय के कण परिक्षेपित कण कहलाते हैं।
आमतौर पर विलयन में जो पदार्थ कम मात्रा में रहता है उसे विलेय और जो अधिक मात्रा में रहता है उसे विलायक कहते हैं।
जलीय विलयन— किसी पदार्थ को जल में घुलाकर जो विलयन बनता है उसे जलीय विलयन कहते हैं।
विलयन के प्रकार
विलयन में घुले विलय की मात्रा के अनुसार विलियम दो प्रकार के होते हैं—असंतृप्त विलयन एवं संतृप्त विलयन।
असंतृप्त विलयन— किसी निश्चित ताप पर बना वह विलयन जिसमें विलेय की और अधिक मात्रा उस ताप पर घुलाई जा सकती है, असंतृप्त विलयन कहलाता है।
संतृप्त विलयन— किसी निश्चित ताप पर बना वह विलयन जिसमें विलेय की अधिकतम मात्रा घुली हो, संतृप्त विलयन कहलाता है।
अतिसंतृप्त विलयन— वह संतृप्त विलयन जिसमें विलेय की मात्रा उस विलयन को संतृप्त करने के लिए आवश्यक विलेय की मात्रा से अधिक घुली हुई हो, अतिसंतृप्त विलयन कहलाता है।
निलंबन— निलंबन एक विषमांग पदार्थ है जिसमें किसी ठोस के पदार्थ के छोटे-छोटे कण द्रव या गैस में घूलते नहीं, बल्कि संपूर्ण द्रव या गैस में निलंबित स्थिति में रहते हैं। जैसे- कीचड़युक्त जल, बालू एवं जल का मिश्रण आदि।
निलंबन के गुण
यह एक विषमांग मिश्रण है।
इसमें ठोस के कण काफी बड़े होते हैं। जिन्हें नंगी आंखों से या माइक्रोस्कोप की सहायता से आसानी से देखा जा सकता है।
ठोस के निलंबित कण छन्ना पत्र को पार नहीं कर सकते हैं। यह अस्थाई होता है। इसमें निलंबित ठोस के कण द्रव से अलग हो जाने की प्रवृत्ति रखते हैं। ये लंबे समय तक निलंबित अवस्था में नहीं रहते हैं।
इसमें निलंबित ठोस के कणों का व्यास 10-5 सेंटीमीटर या इससे अधिक होता है।
ब्राउनी गति— कोलॉइडी विलयन के अंतर्गत कोलॉइड के कण टेढ़े-मेढ़े मार्ग से होकर लगातार गमन करते रहते हैं। जिसे ब्राउनी गति कहा जाता है।
टिंडल प्रभाव— किसी प्रकाश के पुंज को एक कोलॉइडी विलयन से होकर प्रवाहित करने पर किरण-पथ पारभासित हो जाता है। कोलाइड के कण प्रकाश का प्रकीर्णन कर देते हैं। इस घटना को टिंडल प्रभाव कहते हैं।
प्रश्न 1. निम्नलिखित अवलोकनों हेतु कारण लिखें –
(a) नैफ्थलीन को रखा रहने देने पर यह समय के साथ कुछ भी ठोस पदार्थ छोड़े बिना अदृश्य हो जाती है।
(b) हमें इत्र की गंध बहुत दूर बैठे हुए भी पहुँच जाती है।
उत्तर: (a) नैफ्थलीन को रखा रहने देने पर यह ऊर्ध्वपातित हो जाती है, अर्थात यह द्रव अवस्था में परिवर्तित हुए बिना ठोस अवस्था से सीधे गैस में परिवर्तित हो जाती है।
(b) इत्र के कण वायु में मिल जाते हैं और विसरित होकर हम तक पहुँचते हैं। इत्र के कणों की तेज गति और अत्यधिक रिक्त स्थानों के कारण उनका वायु में विसरण बहुत तीव्रता से होता है।
प्रश्न 2. निम्नलिखित पदार्थों को उनके कणों के बीच बढ़ते हुए आकर्षण के अनुसार व्यवस्थित करें।
(a) जल
(b) चीनी
(c) ऑक्सीजन।
उत्तर: पदार्थों का उनके कणों के बीच बढ़ते हुए आकर्षण का क्रम—
ऑक्सीजन < जल < चीनी
प्रश्न 3. निम्नलिखित तापमानों पर जल की भौतिक अवस्था क्या है –
(a) 25°C
(b) 0°C
(c) 100°C
उत्तर: (a) 25°C पर द्रव अवस्था।
(b) 0°C पर द्रव व ठोस दोनों अवस्थाएँ सम्भव हैं।
(c) 100°C पर द्रव व गैस दोनों अवस्थाएँ सम्भव हैं।
प्रश्न 4. पुष्टि हेतु कारण दें –
(a) जल कमरे के ताप पर द्रव है।
(b) लोहे की अलमारी कमरे के ताप पर ठोस है।
उत्तर:
(a) जल कमरे के ताप पर द्रव है क्योंकि इसका एक निश्चित आयतन है व इसमें बहाव है।
(b) लोहे की अलमारी कमरे के ताप पर ठोस है क्योंकि इसका एक निश्चित आकार व आयतन है। इसमें जल की भाँति बहाव नहीं है।
प्रश्न 5. 273K पर बर्फ को ठंडा करने पर तथा जल को इसी तापमान पर ठंडा करने पर शीतलता का प्रभाव अधिक क्यों होता है?
उत्तर: 273 K या 0°C पर ठंडा करने पर बर्फ, जल की तुलना में ज्यादा शीतलता प्रदान करती है, क्योंकि वह जल में परिवर्तित होने के लिए संगलन की प्रसुप्त ऊष्मा जितनी ऊष्मा अवशोषित करती है। जबकि 273 K पर जल की अवस्था में परिवर्तन नहीं होता। अतः यह बर्फ की तुलना में कम ऊर्जा अवशोषित करता है।
प्रश्न 6. उबलते हुए जल अथवा भाप में से जलने की तीव्रता किसमें अधिक महसूस होती है ?
उत्तर: भाप से उबलते हुए जल की तुलना में जलने की तीव्रता अधिक महसूस होती है क्योंकि भाप के कणों में उसी तापमान पर पानी के कणों की अपेक्षा अधिक ऊर्जा होती है। ऐसा इसलिए है, क्योंकि भाप के कणों ने वाष्पीकरण की गुप्त ऊष्मा के रूप में अतिरिक्त ऊष्मा अवशोषित कर ली है।
- गैस का द्रव में बदलना संघनन कहलाता है।
- ठोस का द्रव में बदलना संगलन या द्रवीकरण कहलाता है।
- द्रव का वाष्प में बदलना वाष्पीकरण कहलाता है।
- द्रव का ठोस में बदलना जमना कहलाता है।
- ठोस का सीधे गैस में बदलना ऊर्ध्वपातन कहलाता है।
- गैस का ठोस में बदलना निक्षेपण कहलाता है।
Bottom of Form
प्रश्न 7. पदार्थ से आप क्या समझते हैं ?
उत्तर: जो स्थान घेरे, जिसमें द्रव्यमान हो या आयतन हो, उसे पदार्थ कहते हैं।
प्रश्न 8. समांगी और विषमांगी मिश्रणों में अन्तर बताएँ।
उत्तर: समांगी मिश्रण वह मिश्रण होता है जिसके अवयवों को पृथक रूप से नहीं देखा जा सकता अथवा जिसकी बनावट समान होती है। उदाहरण-जल में नमक व जल में चीनी का विलयन। विषमांगी मिश्रण के अंश भौतिक दृष्टि से पृथक होते हैं। उदाहरण- सोडियम क्लोराइड व लोहे की छीलन, नमक व सल्फर, जल एवं तेल का मिश्रण।
प्रश्न 9. उदाहरण के साथ समांगी एवं विषमांगी मिश्रणों में विभेद कीजिए।
उत्तर:
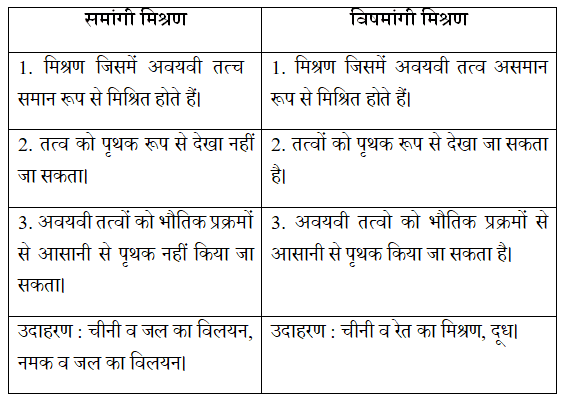
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
प्रश्न 2. विलयन, निलम्बन और कोलाइड एक-दूसरे से किस प्रकार भिन्न हैं ?
उत्तर :
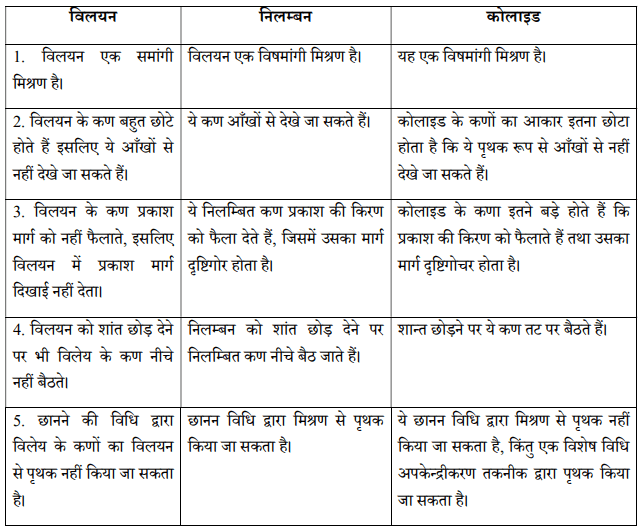
प्रश्न 10. पेट्रोल और मिट्टी का तेल (Kerosene oil) जो कि आपस में घुलनशील हैं, के मिश्रण को आप कैसे पृथक् करेंगे। पेट्रोल तथा मिट्टी के तेल के क्वथनांकों में 25°C से अधिक का अन्तराल है।
उत्तर: पेट्रोल व मिट्टी के तेल को साधारण आसवन विधि द्वारा पृथक् किया जा सकता है क्योंकि मिट्टी का तेल व पेट्रोल गर्म करने पर विघटित नहीं होते व उनके क्वथनांकों के बीच काफी अधिक अन्तराल है।
प्रश्न 11. पृथक् करने की सामान्य विधियों के नाम दें—
1. दही से मक्खन
2. समुद्री जल से नमक
3. नमक से कपूर।
उत्तर:
1. दही से मक्खन-अपकेन्द्रन।
2. समुद्री जल में नमक-आसवन विधि।
3. नमक से कपूर-ऊर्ध्वपातन विधि।
प्रश्न 12. क्रिस्टलीकरण विधि से किस प्रकार के मिश्रणों को पृथक् किया जा सकता है ?
उत्तर: क्रिस्टलीकरण विधि का प्रयोग ठोस पदार्थों को शुद्ध करने में किया जाता है। क्रिस्टलीकरण वह विधि है जिसके द्वारा क्रिस्टल के रूप में शुद्ध ठोस को विलयन से पृथक् किया जाता है। उदाहरण के लिए समुद्री जल से प्राप्त नमक की अशुद्धियों को दूर करने के लिए क्रिस्टलीकरण विधि का प्रयोग किया जाता है।
प्रश्न 13. निम्न को रासायनिक और भौतिक परिवर्तनों में वर्गीकृत करें।
- पेड़ों को काटना
- मक्खन का एक बर्तन में पिघलना
- अलमारी में जंग लगना
- जल का उबलकर वाष्प बनना
- विद्युत तरंग का जल में प्रवाहित होना तथा उसका
- हाइड्रोजन और ऑक्सीजन गैसों में विघटित होना
- जल में साधारण नमक का घुलना
- फलों से सलाद बनाना तथा
- लकड़ी और कागज का जलना।
उत्तर:
भौतिक परिवर्तन –
- मक्खन का एक बर्तन में पिघलना।
- जल का उबलकर वाष्प बनना।
- जल में साधारण नमक का घुलना।
- फलों से सलाद बनना।
- पेड़ों का काटना।
रासायनिक परिवर्तन –
1. अलमारी में जंग लगना। .
2. विद्युत तरंग का जल में प्रवाहित होना तथा हाइड्रोजन और ऑक्सीजन गैसों में विघटित होना।
3. लकड़ी और कागज का जलना।
14. निम्नलिखित को पृथक् करने में आप किन विधियों को अपनायेंगे?
1. सोडियम क्लोराइड को जल के विलयन से पृथक् करने में,
2. अमोनियम क्लोराइड को सोडियम क्लोराइड तथा अमोनियम क्लोराइड के मिश्रण से पृथक् करने में,
3. धातु के छोटे टुकड़ों को कार के इंजन ऑयल से पृथक् करने में,
4. दही से मक्खन निकालने के लिए
5. जल से तेल निकालने के लिए
7. चाय से चाय की पत्तियों को पृथक करने में,
8. बालू से लोहे की पिनों को पृथक् करने में
9. भूसे से गेहूँ के दानों को पृथक करने में,
10. पानी में तैरते हुए महीन मिट्टी के कण को पानी से अलग करने के लिए,
11. पुष्प की पंखुड़ियों के निचोड़ से विभिन्न रंजकों को पृथक् करने में।
उत्तर:
उपर्युक्त को पृथक् करने के लिए हम निम्न विधियों को अपनायेंगे
1. सोडियम क्लोराइड को जल के विलयन से पृथक् करने में-वाष्पीकरण।
2. अमोनियम क्लोराइड को सोडियम क्लोराइड तथा अमोनियम क्लोराइड के मिश्रण से पृथक् करने में-ऊर्ध्वपातन।
3. धातु के छोटे टुकड़े को कार के इंजन ऑयल से पृथक करने में-छानन/अपकेन्द्रन/संघनन।
4. दही से मक्खन निकालने के लिए-अपकेन्द्रन।
5. जल से तेल निकालने के लिए-पृथक्करण कीप द्वारा।
6. चाय से चाय की पत्तियों को पृथक् करने में-छानन विधि।
7. बालू से लोहे की पिनों को पृथक् करने में-चुम्बकीय विधि।
8. भूसे से गेहूँ के दानों को पृथक् करने में-निष्पावन (Winnowing)
9. पानी में तैरते हुए महीन मिट्टी के कण को पानी से अलग करने के लिए-अपकेन्द्रन।
10. पुष्प की पंखुड़ियों के निचोड़ से विभिन्न रंजकों को पृथक करने में-क्रोमैटोग्राफी।
प्रश्न 15. निम्न की उदाहरण सहित व्याख्या करें –
(a) संतृप्त विलयन
(b) शुद्ध पदार्थ
(c) कोलाइड
(d) निलम्बन
उत्तर:
(a) संतृप्त विलयन – दिए गए निश्चित तापमान पर यदि विलयन में विलेय पदार्थ नहीं घुलता है तो उसे संतृप्त विलयन कहते हैं। किसी निश्चित ताप पर उतना ही विलेय पदार्थ घुल सकता है जितनी कि विलयन की क्षमता होती है। चीनी व जल का विलयन 100°C पर एक संतृप्त विलयन होता है क्योंकि इस ताप पर चीनी और अधिक जल में नहीं घुलती।
(b) शुद्ध पदार्थ – एक शुद्ध पदार्थ वह पदार्थ होता है जिसमें मौजूद सभी कण समान रासायनिक प्रकृति के होते हैं। एक शुद्ध पदार्थ एक ही प्रकार के कणों से मिलकर बना होता है। उदाहरण धातुएँ- सोना, चाँदी, आदि। अधातुएँ- हाइड्रोजन, क्लोरीन, ऑक्सीजन, चीनी, आदि।
(c) कोलाइड – कोलाइड वह मिश्रण होता है जिसके कण विलयन में समान रूप से फैले रहते हैं। यह एक विषमांगी मिश्रण होता है। इसके कणों का आकार इतना छोटा होता है कि ये पृथक् रूप से आँखों से नहीं देखे जा सकते। जब इनको शान्त छोड़ दिया जाता है तब ये तल पर बैठते हैं अर्थात स्थायी होते हैं। ये छानन विधि द्वारा मिश्रण से पृथक् नहीं किये जा सकते किन्तु एक विशेष विधि अपकेन्द्रीकरण तकनीक द्वारा पृथक किये जा सकते हैं। उदाहरण-दूध, कोहरा, धुआँ आदि।
(d) निलम्बन – निलम्बन एक विषमांगी मिश्रण है जिसमें विलेय पदार्थ कण घुलते नहीं हैं बल्कि माध्यम की समष्टि में निलम्बित रहते हैं। ये निलम्बित कण आँखों से देखे जा सकते हैं। जब इसे शान्त छोड़ देते हैं तब ये कण नीचे की ओर बैठ जाते हैं अर्थात निलम्बन अस्थायी होता है। छानन विधि द्वारा इन कणों को मिश्रण से पृथक् किया जा सकता है। उदाहरण-गंदला जल तथा बालू, मिट्टी एवं जल का मिश्रण।
प्रश्न 16. निम्नलिखित में से प्रत्येक को समांगी और विषमांगी मिश्रणों में वर्गीकृत करें सोडा जल, लकड़ी, बर्फ, वायु, मिट्टी, सिरका, छनी हुई चाय।
उत्तर: समांगी मिश्रण- बर्फ, सिरका, छनी हुई चाय, सोडा जल, वायु (शुद्ध वायु समांगी है व अशुद्ध वायु विषमांगी) है।
विषमांगी मिश्रण- मिट्टी, लकड़ी।
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
प्रश्न 17. निम्न में से कौन-सी वस्तुएँ शद्ध पदार्थ हैं –
(a) बर्फ
(b) दूध
(c) लोहा
(d) हाइड्रोक्लोरिक अम्ल
(e) कैल्शियम ऑक्साइड
(f) पारा
(g) ईंट
(h) लकड़ी
(i) वायु।
उत्तर:
निम्न वस्तुएँ शुद्ध मानी जाती हैं –
(a) बर्फ
(c) लोहा
(d) हाइड्रोक्लोरिक अम्ल
(e) कैल्शियम ऑक्साइड
(f) पारा।
प्रश्न 18. निम्नलिखित मिश्रणों में से विलयन की पहचान करें–
(a) मिट्टी
(b) समुद्री जल
(c) वायु
(d) कोयला
(e) सोडा जल
उत्तर: निम्न मिश्रण विलयन हैं –
(b) समुद्री जल
(c) वायु
(e) सोडा जल।
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
प्रश्न 19. निम्न में से कौन टिण्डल प्रभाव को प्रदर्शित करेगा?
(a) नमक का घोल
(b) दूध
(c) कॉपर सल्फेट विलयन
(d) स्टार्च विलयन।
उत्तर: कोलॉइड विलयन टिण्डल प्रभाव प्रदर्शित करते हैं। यहाँ दूध व स्टार्च विलयन कोलॉइड हैं। अतः ये टिण्डल प्रभाव प्रदर्शित करेंगे।
प्रश्न 20. निम्नलिखित को तत्त्व, यौगिक तथा मिश्रण में वर्गीकृत कीजिए।
(a) सोडियम
(b) मिट्टी
(c) चीनी का घोल
(d) चाँदी
(e) कैल्सियम कार्बोनेट
(f) टिन
(g) सिलिकन
(h) कोयला
(i) वायु
(j) साबुन
(k) मीथेन
(l) कार्बन डाइऑक्साइड
(m) रक्त।
उत्तर:
तत्त्व – सोडियम, चाँदी, टिन व सिलिकन।
यौगिक – कैल्सियम कार्बोनेट, मीथेन व कार्बन डाइऑक्साइड।
मिश्रण – मिट्टी, चीनी, कोयला, वायु, साबुन व रक्त।
प्रश्न 21. निम्नलिखित में से कौन से परिवर्तन रासायनिक है–
(a) पौधों की वृद्धि
(b) लोहे में जंग लगना
(c) लोहे के चूर्ण तथा बालू को मिलाना
(d) खाना पकाना
(e) भोजन का पाचन
(f) जल से बर्फ बनना
(g) मोमबत्ती का जलना।
उत्तर: निम्न परिवर्तन रासायनिक हैं –
(a) पौधों में वृद्धि
(b) लोहे में जंग लगना
(d) खाना पकाना
(e) भोजन का पाचन
(g) मोमबत्ती का जलना।
Padarth Ka Vargikaran Class 9th Science Notes in Hindi
Read more – Click here
YouTube Video – Click here
Leave a Reply